የውሃ ባህሪዎች-ኢሶቶፕስ እና ሞለኪውላዊ መዋቅር ፡፡
የውሃ ባህሪዎች 1 አጠቃላይ
የውሃ ባህሪዎች 2-አካላዊ እና ኬሚካዊ ባህሪዎች
የውሃ ኢሶቶፒክ ጥንቅር
ውሃ በኒውክሊየሱ ውስጥ ከሚገኙት ፕሮቶኖች ጋር በተያያዙ የኒውትሮን ብዛት እርስ በርሳቸው የሚለያዩ የተለያዩ የኦክስጂን እና የሃይድሮጂን አይዞቶፖች ድብልቅ ነው ፡፡
1H,2 ኤች (ዲቱሪየም)3ሸ (ትሪቲየም)
16O, 17O,18O.
ገለልተኛ ግንኙነቶች እንደሚከተለው ናቸው
ለሃይድሮጂን
2H/1H = 1/6900
3H/1H = 1/10 18
ትሪቲየም ያልተረጋጋ ንጥረ ነገር ነው ፣ ክፍለ ጊዜው (ግማሽ ህይወቱ) 12,5 ዓመታት ነው።
ለኦክስጂን
18O/16አቤቱ = 1/500
17O/16አቤቱ = 1/2500
4 ዋና ዋና ሞለኪውላዊ ዝርያዎች እና ድግግሞቻቸው እንደሚከተለው ናቸው
1H216ኦ = 99,7%
1H2 18 ኦ = 0,2%
1H217ኦ = 0,04%
1HD16ኦ = 0,03%
D216O = በጣም ደካማ
ልዩ ልዩ isotopes በሞለኪውሎች ውስጥ ባለው አካላዊ ባህርያቶች ውስጥ ልዩነቶችን እንዲጨምሩ ያደርጋቸዋል ፣ በተለይም መጠናቸው በተለይም ኬሚካዊ ባህሪዎች ግን እንደዚሁ አንድ ናቸው ፡፡
ከባድ ውሃ ዲ2ኦ በተፈጥሮው ሁኔታ ውስጥ አለ ግን በጣም
ዝቅተኛ. የሚደነቅ ብዛትን ለማግኘት ፣ የአቶቶፒክ መለያየት ቴክኒኮችን ጠንቅቆ ማወቅ አስፈላጊ ነው-የአቶሚክ መሣሪያን ለማዘጋጀት ባለፈው የዓለም ጦርነት ወቅት ይህ መሠረታዊ ፈተናዎች አንዱ ነበር ፡፡
የውሃ የኬሚካል ክፍሎች isotopic ጥንቅር እንደ የሙቀት ያሉ ቴርሞዳይናሚክ መለኪያዎች ግምት ውስጥ ጥቅም ላይ ይውላል;
ሪፖርቱ 18 O/16O ከዋልታ ክዳን ውስጥ በረዶ እና ከቅሪተ አካል የከርሰ ምድር ውሃ ያለፈውን የአየር ንብረት መረጃ ይሰጣል ፡፡
የውቅያኖስ ውሃ ትነት በአይዞቶፒክ ክፍልፋይ ይከሰታል-ቀላል የኦክስጂን ኦዞን ለከባድ isotope ይተናል ፡፡ ውቅያኖሶች በደመና እና በዝናብ ከሚመጣ ውሃ ይልቅ በከባድ አይዞቶፖች የበለፀጉ ናቸው ፡፡
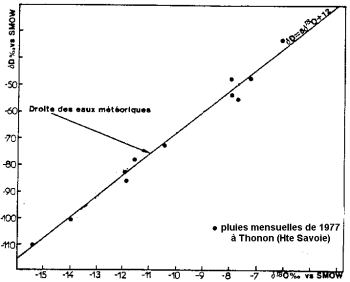
የተረጋጋ የኢሶቶፕ ይዘት (ከ Blavoux እና Letolle ፣ 1995 በኋላ)።
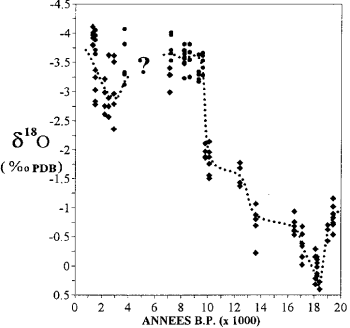
በማዮቴ ውስጥ በሚገኙት ኮራሎች ውስጥ የኦክስጂን ኢሶቶፕ ይዘት ልዩነት (ከካዛኖቫ እና ሌሎች በኋላ ፣ 1994) ፡፡
የሞለኪውል አወቃቀር
ሃይድሮጂን እና ኦክስጅን አቶሞች ኤሌክትሮኖቻቸውን ያሰባስባሉ እንደ ኒዮን ያለ የተሟላ ሽፋን ይፈጥራሉ ፡፡ በእርግጥ የኦክስጂን አቶም የኤሌክትሮኒክ ቅርፊቱን ለማጠናቀቅ 2 ኤሌክትሮኖች የሉትም ፣ እሱ የሚያቀርበው 2 ሃይድሮጂን አቶሞች ናቸው ፡፡ የተፈጠረው H2O ሞለኪውል የተረጋጋ ነው ፡፡
ኦክስጅን: 8 ፕሮቲኖች + 8 ኒውትሮን
ሃይድሮጂን: 2 (2 * (1 ፕሮቶን + 1 ኒትሮን))
ጠቅላላ 10 የ 10 ኤሌክትሮኖች ክሶች ሚዛን በመጠበቅ ላይ።
የሃይድሮጂን ኒውክሊየኖች “የሚኪ ጭንቅላት” (ሃይድሮጂን ጆሮዎች ናቸው) አንድ ባህሪ ለመፍጠር ከኦክስጂን አንድ ጎን አላቸው ፡፡
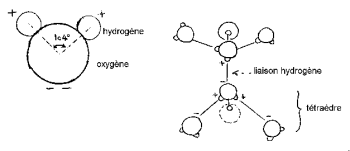
የ HOH አንግል 104,474 ° ነው (የአራትዮሽ ጂኦሜትሪ ባሕርይ)። በእንፋሎት ውስጥ በኦክስጂን እና በሃይድሮጂን አቶም መካከል ያለው ርቀት ወደ 1 A ° (0,95718 A °) ቅርብ ነው። የሞለኪውል ውጤታማ ዲያሜትር የ 2,82 A ° ቅደም ተከተል ነው።
በዚህ አነስተኛ ሞለኪውል ውስጥ የኤሌክትሪክ ክፍያዎች ባልተስተካከለ ሁኔታ ተሰራጭተዋል ፡፡ ኤሌክትሮኖች ከሃይድሮጂን አቶም ይልቅ ወደ ኦክስጅን አቶም በጣም ይሳባሉ ፡፡ በሃይድሮጂን ኒውክሊየስ አቅራቢያ የሚገኙ አዎንታዊ ክፍያዎች 2 ማዕከሎች እና በኦክስጂን ኒውክሊየስ አቅራቢያ ያሉ አሉታዊ ክፍያዎች 2 ማዕከሎች አሉ ፡፡ በክፍያ ስርጭቱ ውስጥ ያለው ይህ ሚዛን መዛባት ፣ ከውሃ ሞለኪውል ቀጥተኛ ያልሆነ ጂኦሜትሪ ጋር ተዳምሮ ጠንካራ የኤሌክትሪክ ዲፖል አፍታ መኖሩን ያሳያል ፡፡ የውሃ ሞለኪውል ዋልታ ነው; እሱ ከሌላው የዋልታ ሞለኪውሎች ጋር ሊያገናኝ የሚችል እንደ ኤሌክትሪክ ዲፖል ይሠራል። በእውነቱ የውሃ ሞለኪውሎች በተቃራኒው የኤሌክትሪክ ክፍያ ክፍላቸውን ወደ እነሱ በመመራት በክሪስታል ንጥረ ነገር አየኖች መካከል ሊገቡ ይችላሉ ፡፡ የክሪስታል ion ቶች መስህብ በጣም የተዳከመ እና የ ‹ክሪስታል› ትስስር ይቀነሳል ፣ ይህም እንዲፈርስ ያመቻቻል ፡፡ የውሃ ሞለኪውል የዋልታ ባህሪዎች የማይክሮዌቭ ማሞቂያ ዘዴን ያብራራሉ ፡፡ በእርግጥ ፣ አንድ የፖላራይዝድ ሞለኪውል ራሱን ከኤሌክትሪክ መስክ ጋር ያገናኛል ፡፡ ይህ ከተለወጠ ሞለኪውል የአቅጣጫ ለውጥን ይከተላል። ከተወሰነ ድግግሞሽ ፣ ጥቂት ጊሄዝ ለውሃ ፣ የሞለኪውሎች እንቅስቃሴ በሙቀት ይሞቃል ፡፡ የቤት ምድጃዎች በተለምዶ በ 2,45 ጊኸር ድግግሞሽ ይሰራሉ ፣ ይህም ዩኤችኤፍ ነው ፡፡
3 የሞለኪዩል ኒውክሊየኖች ቋሚ አይደሉም ፣ እነሱ እርስ በእርስ ይዛመዳሉ ፣ ሞለኪዩሉ ይንቀጠቀጣል እና ይሽከረከራል ፡፡ በፈሳሽ ውሃ ውስጥ ሞለኪውሎች የመቀላቀል አዝማሚያ አላቸው-የማይኪ ጭንቅላት በሃይድሮጂን ትስስር አማካኝነት ጆሮውን ከአገጭ ጋር ያያይዙታል ፡፡ በእርግጥ ከ 8 ቱ የኦክስጂን ኤሌክትሮኖች ውስጥ ከሃይድሮጂን አተሞች ጋር በጋር ትስስር ውስጥ የሚሳተፉት 4 ቱ ብቻ ናቸው ፡፡ ቀሪዎቹ 4 ኤሌክትሮኖች ነፃ ኤሌክትሮን ድብልቶች ተብለው በ 2 ጥንዶች ይመደባሉ ፡፡ እያንዳንዳቸው በአሉታዊ በኤሌክትሪክ ኃይል የተሞሉ ድብልቆች በአቅራቢያ ከሚገኘው የውሃ ሞለኪውል በአዎንታዊ ኃይል ከተሞላ የሃይድሮጂን አቶም ጋር የኤሌክትሮስታቲክ ትስስር መፍጠር ይችላሉ ፡፡ በቤት ሙቀት ውስጥ የተረጋጋ የሃይድሮጂን ትስስር ከኮቭቫል ትስስር ጋር ሲወዳደር ግን ደካማ ነው ፡፡ በውሃ ሞለኪውል ውስጥ ፣ በ 2 ቱ የጋራ ትስስር እና በ 2 ነፃ የኤሌክትሮኒክስ ድብልቆች የተገነባው ጂኦሜትሪ ማዕከሉ በኦክስጂን ኒውክሊየኖች ከተያዘው ቴትራኸድ ጋር ይቀራረባል ፡፡
ሆኖም የውሃ ሞለኪውል መጠነ-ሰፊ መዋቅር አሁንም ፍጽምና የጎደለው ነው ፡፡ የኤክስሬይ እና የኒውትሮን ስርጭት ልዩ እይታ 2 ዋና እሴቶችን ይሰጣል-ከ 1 A ° ጋር የሚመጣጠን ምልክት ፣ በሃይድሮጂን እና በኦክስጂን ኒውክላይ መካከል ያለው ርቀት እና ከሙቀት መጠን እና ከ 2,84 እስከ 4 A ° እሴት ይለያያል ፡፡ በ 2 የኦክስጂን ኒውክላይ መካከል ካለው ርቀት ጋር የሚዛመድ። RX diffractometry በተጨማሪ ከተሰጠው ሞለኪውል ርቀቱ ባለው ርቀት ውስጥ የሚገኝ የአንድ ፈሳሽ መጠን አማካይ የሞለኪውሎችን ብዛት ለማወቅ ያስችለዋል ፡፡ የውሃ ሞለኪውል በአማካኝ 4,4 ጎረቤቶች አሉት ፣ ይህም የአራት እግር ጥልፍልፍን ያሳያል ፡፡ በሃይድሮጂን ትስስር ከተገናኙ ሞለኪውሎች በተጨማሪ ሌሎች የማይወጡ ሞለኪውሎች አሉ ፣ እነሱም በአጎራባች ሞለኪውሎች ቁጥር በትንሹ ከ 4 ለምን እንደሚበልጥ እና በትክክል በአራት ቴሌቴድራል ክሪስታልዝድ ሁኔታ እንደሚፈለገው 4 አይሆኑም ፡፡ በሃይድሮጂን ትስስር የተገናኙ ሞለኪውሎች ክሪስታል ፋትስ የማይወጡ ሞለኪውሎች የሚቀመጡባቸው ክፍተቶችን ይፈጥራሉ ፡፡ ሌላ መላምት በሃይድሮጂን ትስስር መዛባት ላይ የተመሠረተ ነው ፡፡ የኋለኛው ፣ መጀመሪያ መስመራዊ ፣ ማለትም ከ ‹ኦ- HO› አተሞች ጋር የተዛመደ ነው ማለት ፣ የተለያዩ ደረጃዎችን በማዞር ከቅርብ ጎረቤቶች የበለጠ ርቀው የሚገኙ ሞለኪውሎች ወደ ማዕከላዊ ሞለኪውል እንዲቀርቡ ያስችላቸዋል ፡፡
የፅንሰ-ሀሳባዊ ሞዴሎች በቅርብ ጊዜ ኃይለኛ ኮምፒተርን በመጠቀም ተዘጋጅተዋል ፡፡ እነሱ ወደ 80% የሚሆኑት የውሃ ሞለኪውሎች በ 3 ወይም በ 4 የሃይድሮጂን ትስስር ውስጥ እንደሚገኙ ያመለክታሉ ፡፡ በሌላ በኩል ደግሞ የማይለወጡ ሞለኪውሎች መኖራቸውን ያስወግዳሉ ፡፡ የኮምፒተር ሞዴሊንግ እንደሚያሳየው ውሃው በሚቀዘቅዝበት ጊዜ የሞለኪውሎች አውታረመረቦች ከአይስ ጋር ከሚመሳሰሉት ሄክሳጎን ጋር እየጨመረ ይመሳሰላሉ ፡፡
ጠንካራው ሁኔታ ከተጠናከረ ክሪስታል ቅንጅት ጋር ይዛመዳል። በተለመደው ግፊት ፣ በረዶ ባለ ስድስት ጎን ቅርፅ አለው ፡፡ በዝቅተኛ የሙቀት መጠን (-80 ° ሴ በታች) አንድ ኪዩብ መዋቅር ሊወስድ ይችላል ፡፡ የኤሌክትሪክ ክፍያዎች በክሪስታል መተላለፊያው ውስጥ ሊንቀሳቀሱ እና ionic ዓይነት ክሪስታል ጉድለቶችን ሊያወጡ ይችላሉ-የውሃ ፈሳሽ ፕሮቶን H3O + እና hydroxyl ion OH- ፡፡ የበረዶው ክሪስታል ፋትታ ሞለኪውሎች በጣም ሊጣበቁ ከሚችሉት መደራረብ ጋር አይዛመድም ፡፡ ውህደት ላይ ፣ የሃይድሮጂን ትስስሮች ስለሚሰበሩ እና ሞለኪውሎቹ አንድ ላይ ስለሚቀራረቡ ጉድለቶቹ ይወድቃሉ-መጠናቸው እስከ 4 ° ሴ ቢበዛ ይጨምራል ፡፡ በመቀጠልም በፈሳሽ ውሃ ውስጥ የሙቀት መጠን መጨመር ሞለኪውሎችን ይገፋፋቸዋል እንዲሁም መጠናቸው ይቀንሳል ፡፡
የበለጠ ለመረዳት ፣ ማጣቀሻዎች እና መጽሃፍ ቅዱሳዊ ጽሑፎች-
Blavoux B. and Letolle R. (1995) - የከርሰ ምድር ውሃ ዕውቀትን በተመለከተ የአይሶቶፕ ቴክኒኮች አስተዋፅዖ ፡፡ ጂኦክሮኒክስ ፣ 54 ፣ ገጽ 12-15 ፡፡
ካሮ ፒ (1990) - የውሃ አካላዊ እና ኬሚካዊ ባህሪዎች ፡፡ ታላቁ የውሃ መጽሐፍ ፣ ላ ቪሌት ፣ ገጽ. 183-194 እ.ኤ.አ.
ኤግላንድ ዲ (1990) - የውሃ አወቃቀር ፡፡ ላ ሬቼቼ ፣ 221 ፣ ገጽ 548-552 እ.ኤ.አ.
ማይደንት ዲር (1992) - የሃይድሮጅኦሎጂ መመሪያ መጽሐፍ ፡፡ ማክ ግራው ሂል.
ካዛኖቫ ጄ ፣ ኮሎንና ኤም እና ድጄሩድ ኬ. (1994) - ጂኦፕሮሰፕፔፕ - ፓሊኦኮማቶሎጂ ፡፡ ራፕ ሳይንቲስት BRGM ፣ ገጽ 76-79 ፡፡

